پتاسیم دیکرومات که به آن پتاسیم بی کرومات نیز گفته میشود، دارای فرمول شیمیایی K2Cr2O7 است. یون دی کرومات یک نوع آنیون چند اتمی با فرمول شیمیایی Cr2O2−7 است. ترکیبات یونی حاوی این یون در شمار عوامل اکسید کننده نسبتاً قوی طبقه بندی میشوند و عدد اکسایش پتاسیم دی کرومات 6 است. در محلولهای آبی، یون کرومات با فرمول CrO2−4 و دیکرومات میتوانند به صورت برگشت پذیر به هم تبدیل شوند. یک ماده معدنی رایج است که بیشتر به عنوان اکسید کننده در کاربردهای مختلف آزمایشگاهی و صنعتی استفاده میشود.
فروش دی کرومات پتاسیم
این محصول به صورت پروفرمایی با تضمین کیفیت مطابق با آنالیز ارائه شده از کشور چین وارد شده و به فروش میرسد.
خرید پتاسیم دی کرومات
شما میتوانید جهت کسب اطلاعات بیشتر در مورد نحوه ثبت سفارش، واردات مواد شیمیایی و فروش پروفرمایی مواد شیمیایی مورد استفاده در صنایع با کارشناسان ما در شرکت پترو کیمیا تماس حاصل فرمائید.
خواص فیزیکی و شیمیایی
چگالی آن 676/2 گرم بر میلیلیتر است که بیشتر از چگالی آب است. از دیگر خصوصیات فیزیکی آن این است که بی بو و محلول در آب است. در دما و فشار محیط پایدار است، و با موادی که به عنوان عامل کاهنده عمل میکنند اصلا دوست نیست چرا که پتاسیم دی کرومات خود یک ماده اکسنده بسیار قوی است. اکسید کننده قوی به ترکیباتی گفته میشود که خاصیت اشتعال پذیری سایر مواد را با استفاده از اکسیژن افزایش میدهد. از این رو، پتاسیم دی کرومات باید از این مواد کاهنده و همچنین و سایر مواد ناسازگار با آن دور باشد چراکه امکان دارد یک وضعیت انفجاری ایجاد شود.
| فرمول شیمیایی | K2Cr2O7 |
| جرم مولی | 294.185 g/mol |
| شکل ظاهری | کریستال قرمز مایل به نارنجی بدون بو |
| دانسیته | 2.676 g/cm3, solid |
| نقطه ذوب | 398 °C (748 °F; 671 K) |
| نقطه جوش | 500 °C (932 °F; 773 K) decomposes |
| حلالیت در اب | 4.9 g/100 mL (0 °C) 13 g/100 mL (20 °C) 102 g/100 mL (100 °C) |
| حلالیت در سایر حلال ها | نا محلول در الکل و استون |
| ساختار شیمیایی | 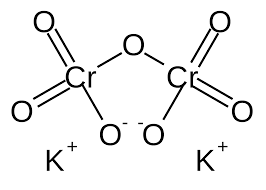 |
کاربرد پتاسیم دی کرومات
عنصر شیمیایی پتاسیم برای طیف گستردهای از عملکردهای بیولوژیکی در بدن انسان کاربرد دارد ولی ترکیب شیمیایی این ماده کاملا برعکس است و برای سلامتی انسان بسیار مضر است.
پتاسیم دی کرومات بسیار خورنده است و یک ماده اکسید کننده بسیار قوی است و از این ویژگی آن در کاربردهای مختلفی استفاده میشود.
- این ترکیب شیمیایی معمولا به عنوان معرف شیمیایی معدنی برای فرآیندهای صنعتی و آزمایشگاهی مورد استفاده قرار میگیرد.
- این ماده شیمیایی برای تولید محصولاتی مانند واکس کفش و چسب تا تولید رنگدانه و فرآیندهای فوتوشیمیایی مورد استفاده قرار میگیرد.
- سدیم دی کرومات دارای طبیعت بسیار خورنده است و یک عامل اکسید کننده قوی است. این ماده معمولاً برای تولید سایر ترکیبات کروم استفاده می شود.
- در حفاری گل و لای، نگهدارنده های چوب، سیمان و به عنوان مهار کننده خوردگی فلزات استفاده می شود.
- از این ماده برای تهیه محلولهای تمیز کننده قوی برای ظروف شیشهای و مواد چدنی استفاده میشود.
- این ماده شیمیایی در فرآیند گالوانیزه در مخزن خنک کننده نیز کاربرد دارد.
واکنش تهیه دی کرومات پتاسیم
K2Cr2O7 از طریق واکنش کلرید پتاسیم (KCl) با سدیم دیکرومات (Na2Cr2O7) و به دنبال آن خنک کردن و کریستال سازی تبخیری به صورت صنعتی تولید میشود.
Na2Cr2O7 2KCl → K2Cr2O7 2NaCl
یکی دیگر از راههای تولید این محصول واکنش بین محلول تری اکسید کروم و پتاسیم هیدروکسید است که محصولات این واکنش از خلوص بالای برخوردارند.
یک راه دیگر برای تولید این محصول واکنش بین مواد مرتبط با آن مانند پتاسیم کرومات (K2CrO4) و اسیدهایی است که نمک دیکرومات حاصل میکنند.
واکنش های پتاسیم دی کرومات
واکنش تجزیه پتاسیم دی کرومات
این نمک پتاسیم خیلی سریع در آب یونیزه میشود و یونهای کرومات (CrO42-) و دیکرومات (Cr2O72-) در تبادل تولید میشود. در شرایط عادی پایدار است اما بر اثر حرارت دیدن مطابق واکنش زیر، پتاسیم کرومات (K2CrO4) و کرومیک آنهیدرید (CrO3) و اکسیژن تولید میکند.
4K2Cr2O7 → 4K2CrO4 2Cr2O3 3O2
واکنش با پتاس
با انجام واکنش برگشتپذیر با مواد پایهای مانند پتاس (K2CO3) یک محلول زرد رنگی از نمکهای کرومات تولید میشود.
K2Cr2O7 K2CO3 → 2K2CrO4 CO2
واکنش پتاسیم دی کرومات با اسید سولفوریک
این ماده با اسیدهای رقیق سرد واکنش میدهد و کرومیک آنهیدرید تولید میکند و در صورت واکنش با اسیدهای غلیظ نمکهای کرومات و اکسیژن تولید میکند. از واکنش پتاسیم دی کرومات با اسید سولفوریک انیدرید کروم با فرمول شیمیایی CrO3 که به شکل کریستال قرمز رنگ است تولید میشود.
آسیب ها و خطرات
این ماده در درجه اول بر دستگاه تنفسی تاثیر میگذارد و باعث ایجاد زخم، تنگی نفس، برونشیت، ذاتالریه و آسم میشود اما میتواند بر دستگاه گوارش، کبد، کلیهها و سیستم ایمنی نیز تاثیرگذار باشد. این ماده به عنوان یک ترکیب کروم دار شش ظرفیتی بسیار سرطانزا برای انسان شناخته شده است و باعث افزایش خطر ابتلا به سرطان ریه و سرطان حفره سینوسی میشود. در صورت تماس پوستی باعث تحریک شدید و احساس سوزش میشود و حتی ممکن است منجر به کوری شود. همچنین محققان یافتهاند که میتواند بر روی سلامت تولید مثل تاثیر گذار باشد و به عنوان یک عامل جهشزا عمل کند به این معنا که روی ژنتیک تاثیر میگذارد و به کودکان نابالغ آسیب میزند.
MSDS پتاسیم دی کرومات
- در صورت لزوم از تجهیزات محافظت شخصی استفاده کنید.
- صورت، دستها و هر قسمت از بدن که درمعرض آن قرار گرفته باید به طور کامل شسته شود.
- هنگام استفاده از این محصول از خوردن، آشامیدن و سیگار کشیدن پرهیز کنید.
- از تنفس گرد و غبار، بخار و اسپری آن پرهیز کنید.
- فقط در بیرون یا در محیطی با تهویه مناسب استفاده شود.
- از در معرض گرما قرار گرفتن، جرقه، شعله باز و تماس با جسم داغ خوداری شود.
- قبل از مصرف برگه ایمنی این محصول مطالعه شود.
واردات مواد شیمیایی و فروش پروفرمایی
شرکت پترو کیمیا به عنوان وارد کننده مواد شیمیایی به صورت پرفرمایی از کشور چین افتخار تامین بخشی از نیاز مصرف کنندگان در کشور را دارد. شما میتوانید جهت کسب اطلاعات بیشتر در مورد واردات مواد شیمیایی و فروش پروفرمایی مواد اولیه شیمیایی با مشاوران ما در شرکت پترو کیمیا تماس حاصل فرمائید.
فروش پروفرمایی پتاسیم دی کرومات در پترو کیمیا


















نقد و بررسیها
هنوز بررسیای ثبت نشده است.