آمونیاک (Ammonia) که به نام های اندروس، هيدروكسيد اندروس آمونيوم و هيدروژن نيتريد معروف است، یک گاز بی رنگ تشکیل شده از نیتروژن و هیدروژن با بوی تند بوده که بسیاری از نیاز های غذایی موجودات را برطرف میکند. مقدار طبیعی این ماده بسیار کم بوده و در اثر تجزیه مواد الی موجود در گیاهان و حیوانات تولید میشود. این ماده در حالت های جامد، مایع و گاز پایدار است، البته در حالت استاندارد به شکل گازیست و دمای جوش 34/33- درجه سانتی گراد دارد که برای تبدیل آن به مایع باید فشار را افزایش یا دما را کاهش داد و با استفاده از یخ خشک نیز سریعا این عمل انجام خواهد شد.
برای تهیه آمونیاک در خانه از غلظت 5 الی 10 درصد این ماده استفاده میشود که به عنوان یک ماده پاک کننده برای شستشو و برطرف کردن لکه ها از سطوح مختلف در منزل به عنوان آمونیاک خانگی کاربرد دارد.
فهرست عناوین
Toggleتولید با فرایند بوش – هابر
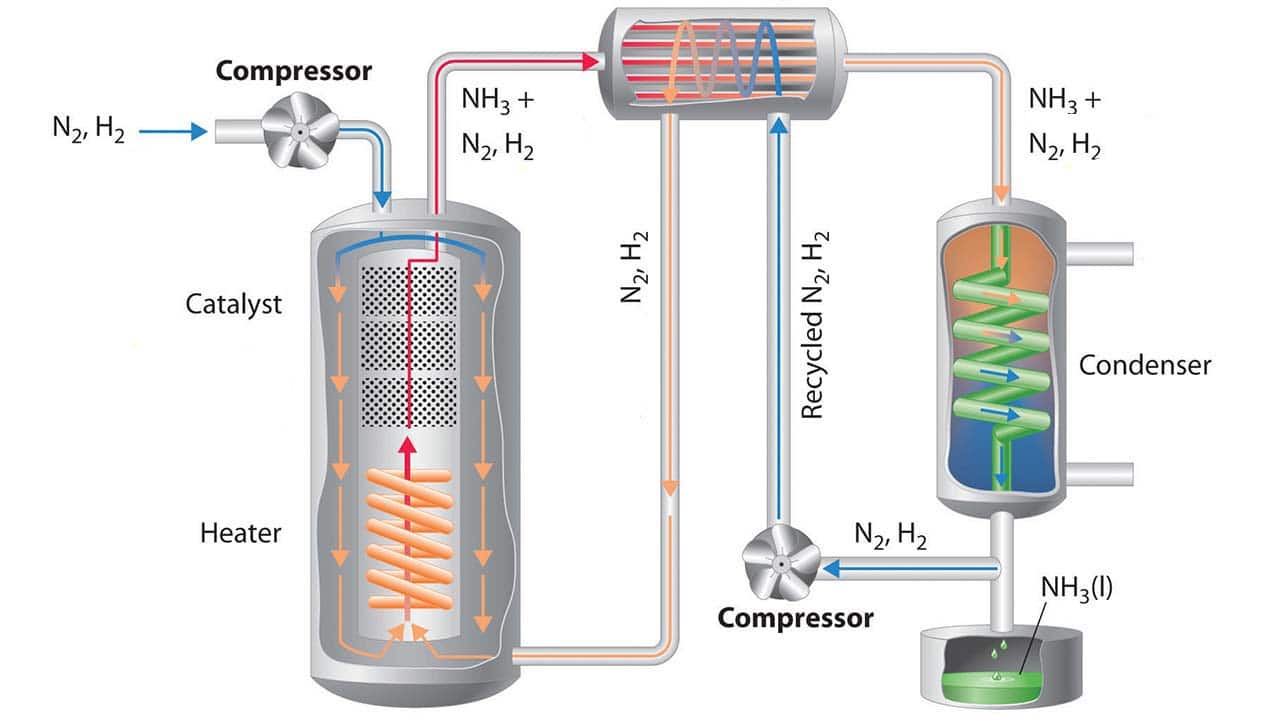
بهترین روش برای تولید آمونیاک روش هابر- بوش است که درآن با اعمال دما و فشار بالا در حضور کاتالیست آهن، نیتروژن هوا را با هیدروژنی که حاصل از برهم کنش گاز طبیعی و بخار آب است واکنش می دهند.
N2 (g) + 3H2 (g) ↔ 2NH3 (g) + q
این فرایند سالانه 450 میلیون تن آمونیاک و مشتقات آن را تولید میکند که باعث افزایش بهره وری زمین های کشاورزی میشود.
تولید و استفاده ی بیش از حد از آمونیاک خطراتی از جمله افزایش میزان نیترات در سفره های آب زیرزمینی و آب های جاری و در نتیجه آسیب رساندن به سلامت موجودات و کاهش کیفیت آب و همچنین افزایش گاز گلخانه ای نیتروس اسید را به دنبال خواهد داشت.
بیشتر بخوانید: کود شیمیایی چیست؟
خواص کاربردی آمونیاک
برخی از خواص منحصر به فرد NH3 آن را به ماده ای اساسی در آزمایشگاه و صنعت برای تولید انواع مواد تبدیل کرده است، از جمله:
هیدروژن نیترید خاصیت بافری داشته و در ثابت نگه داشتن pH موثر واقع می شود. این ماده در واکنش های جایگزینی هسته دوستی موجب تولید آمین ها و در اثر واکنش با کربوکسیلیک اسید یا استر و انیدرید موجب تشکیل آمید ها می شود. NH3 گاهی به عنوان لیگاند عمل کرده و بسیاری از ترکیبات معدنی و کمپکس ها را ایجاد میکند. همچنین هیدروژن موجود در آن نیز در بسیاری از واکنش های جانشینی موثر بوده و باعث تولید محصولات مختلف خواهد شد.
کاربردهای آمونیاک
این ماده تشکیل شده از نیتروژن و هیدروژن؛ کاربردهای متنوعی خصوصا در تولید سایر مواد و محصولات شیمیایی دارد که در ادامه به برخی از آنها خواهیم پرداخت:
نقش آمونیاک در تولید کود
عمده ترین کاربرد آمونیاک در تولید کود است که تاثیر به سزایی در رشد محصولات کشاورزی ایفا میکند و طبق واکنش زیر کود اوره تولید می شود.
2NH3 + CO2 —> (NH2)2CO + H2O
NH3 بهترین گزینه برای تولید کود و تامین نیترات مورد نیاز گیاهان است زیرا به سرعت با خاک ترکیب شده و تولید نیتروژن به فرم یونی میکند که گیاه می تواند مستقیما از آن تغذیه کند و علاوه بر موثر بودن در رشد، باکتری ها و آفات را نابود میکند.
بیشتر بخوانید: کود فسفر چیست؟
کاربرد آمونیاک در صنعت
- در تولید بسیاری از مواد ازته موثر است و یکی از مهم ترین پیش ماده ها برای تولید نیتریک اسید محسوب میشود، همچنین این ماده پیش ماده ی بسیاری از مواد شیمیایی از جمله هیدرازین، اوره و فنل در صنایع و حتی اسید آمینه و نوکلئوتید در بدن است.
- به صورت هیدروکسید آمونیوم یا همان NH3 محلول در آب با غلظت پایین در مصارف خانگی کاربرد دارد که علاوه بر پاک کردن سطوح باعث ایجاد درخشش نیز میشود.
- در صنعت تخمیر، نیتروژن مورد نیاز میکروارگانیسم ها را تامین کرده و PH را در سطح مطلوب حفظ میکند.
- نوع تجاری و خالص که به آمونیاک بدون آب معروف است یکی از کاربردی ترین مواد برای کاهش الودگی میکروبی در گوشت گاو است.
- به دلیل میزان اکتان بالا میتواند به عنوان جایگزینی برای سوخت های فسیلی هم کاربرد داشته باشد که در اثر سوختن، اکسید های کربن تولید نمیکند. از معایب این روش این است که به دلیل دمای پایین شعله قدرت پایینی در موتور ایجاد خواهد شد.
- در ساخت ویتامین B و سولفونامید ها در داروسازی کاربرد دارد.
- در استخراج نیکل و روی و تصفیه آب و کنترل الودگی هوا هم مورد استفاده قرار میگیرد.
- از این ماده در سیستم های تبرید، پاکسازی SO2 تولید شده از سوخت های فسیلی، سوخت در موتور موشک ها، تصفیه ی مواد پنبه ای، تیره سازی چوب بلوط برای طراحی منسوجات چوبی و… استفاده میشود.
خطرات آمونیاک
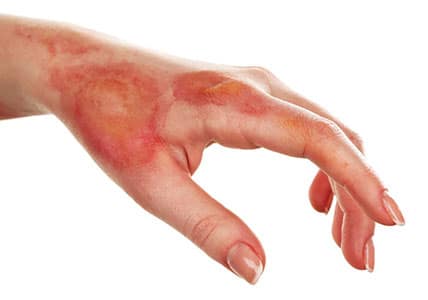
NH3 در دسته ی مواد بسیار اشتعال پذیر قرار نمیگیرد اما در صورتی که ظروف آن در معرض حرارت زیاد باشند منفجر خواهد شد. این ماده زمانی که به شکل غلیظ و مایع باشد بسیار خطرناک بوده و خاصیت سوزانندگی دارد. هنگامی که در تماس با پوست، چشم یا دهان قرار بگیرد، در اثر واکنش با رطوبت موجود در بافت ها امونیوم هیدروکسید که ماده ای سوزاننده است تولید میکند و باعث اسیب به لیپید های موجود در غشای سلول و در نتیجه التهاب میشود.
استنشاق در غلظت های پایین باعث سرفه و تحریک دستگاه تنفسی و استنشاق غلظت های بالا به دلیل خورندگی باعث سوختن بینی و آسیب جدی به مجاری تنفسی خواهد شد. استنشاق آمونیاک همچنین میتواند خستگی بیش از حد نیز ایجاد کند.
در صورتی که این ماده در غلظت های کم با چشم یا پوست در ارتباط باشد باعث التهاب و سوزش انها و در صورت بالا بودن غلظت باعث سوختگی پوست و نابینایی خواهد شد. بلع هیدروژن نیترید باعث خوردگی و اسیب به بافت های داخلی میشود. برای درمان اسیب های جزئی ناشی از آمونیاک باید محل اسیب دیده با مقدار زیادی آب شستشو داده شود و در صورت بلع نوشیدن شیر هم می تواند موثر باشد.
سوالات متداول
در ادامه به برخی از سوالات متداول در این زمینه می پردازیم.
۱-آمونیاک اسید است یا باز؟
این ماده به عنوان یک باز ضعیف با اسیدها واکنش می دهد و تولید نمک میکند، همچنین میتواند با از دست دادن پروتون خود و تبدیل شدن به NH2– در نقش اسید ضعیف عمل کند.
۲-محلول خانگی آمونیاک چیست؟
محلول خانگی آمونیاک در واقع یک محلول آبی از آمونیاک است که در آن آمونیاک کاملا رقیق شده و به غلظتی در حدود ۵ تا ۱۰ درصد می رسد. از این محلول به عنوان پاک کننده و ضدعفونی کننده استفاده می شود.
۳-آمونیاک خون چیست؟
در بدن ما همواره مقداری آمونیاک به طور طبیعی تولید می شود که مقادیر کم آن مشکلی ایجاد نمی کند و حتی می تواند برای بدن مفید باشد. اما در برخی موارد افزایش مقدار آمونیاک خون می تواند موجب بیماری های خونی، ایجاد مشکلات مغزی، کما و در برخی موارد مرگ شود.
۴-کاربرد آمونیاک در ورزش چیست؟
از آمونیاک در ورزش جهت افزایش هوشیاری و تمرکز استفاده می شود. آمونیاک بوی تندی دارد و می تواند به افزایش تمرکز ورزشکاران کمک کند. اما در غلظت های بالا می تواند موجب آسیب به سیستم تنفسی و مشکلات ریوی شود.